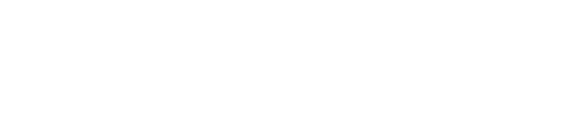第一作者:李哲
通讯作者:吴轩浩/吴忠标
通讯单位:浙江大学
DOI:10.1038/s41467-025-67244-z
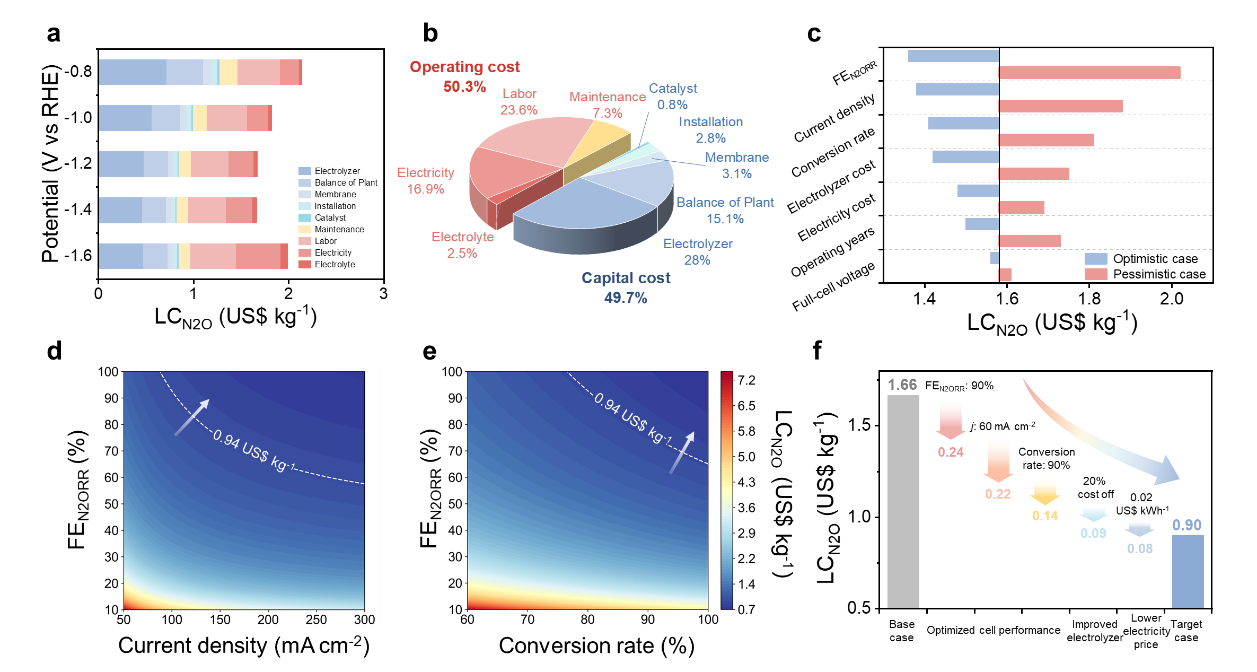
氧化亚氮(N2O)是仅次于二氧化碳和甲烷的第三大温室气体,其全球变暖潜势(GWP)可达CO2的273倍,并能显著破坏臭氧层,已被视为21世纪主要的人为臭氧消耗物质之一。工业排放(如己二酸、硝酸生产尾气)是其重要人为来源,这类废气中N2O浓度较高(0.3~40 vol.%)、排放集中,适宜进行定向治理。目前广泛采用的热催化技术存在能耗高、碳排放量大、催化剂易失活等局限,因此迫切需要发展低温、高效且可持续的新型减排途径。电催化N2O还原反应作为一种环境友好、可在温和条件下进行的替代技术,显示出良好前景,但面临单程转化率低(通常<30%)的瓶颈。该问题主要源于两方面:一是反应器内传质效率低,传统电解池中N2O溶解度有限、扩散路径长;二是催化剂本征活性不足,N2O分子化学惰性强,其在催化剂表面的吸附与活化过程能垒较高,后续N–O键加氢断裂步骤动力学缓慢。这些因素共同制约了该技术的整体转化效率与实际应用可行性。
本研究开发了一种基于CuAg双金属纳米合金催化剂的气体扩散电解池(GDE)系统,用于高效电催化还原N2O为N2。在10 vol.% N2O的工业浓度条件下,系统实现了79.4%的单程转化率及1381.7 μmol h-1 mgcat-1的高分解速率。计算流体动力学模拟表明,该体系通过优化气体流动与扩散路径,显著提升了N2O在电极表面的分布均匀性,克服了传统间歇式反应器的传质限制。Cu与Ag之间的电子协同效应强化了N2O的吸附、加氢及N–O键的解离。技术经济评估显示,该工艺的平准化分解成本为1.66~2.14 $ kg-1。该研究凸显了电催化N2O分解技术的应用潜力与工程可行性。
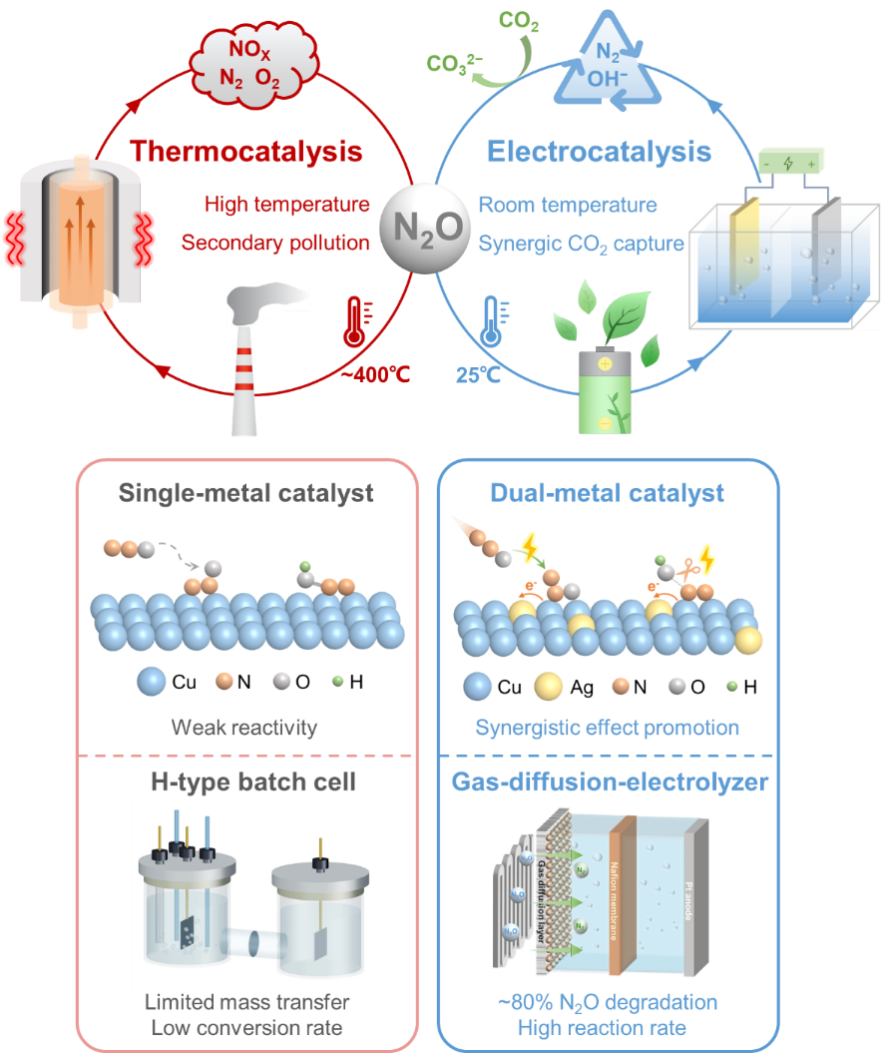
图1 CuAg双金属纳米合金催化剂-气体扩散电解池体系电催化N2O还原示意图。
图2 CuAg/MWCNT催化剂理化表征及其N2ORR性能。(a)CuAg催化剂合成示意图。(b)催化剂TEM图像和粒径分布。(c)催化剂EDS元素分布图。(d)GDE的示意图和气体扩散机制,以及工作电极SEM图像。(e)催化剂的反应速率拟合曲线。(f)在GDE和H型电解池中的N2O转化率对比。(g)CuAg催化剂在不同电位下的10 vol.% N2O转化率和(h)法拉第效率(FEN2ORR)。
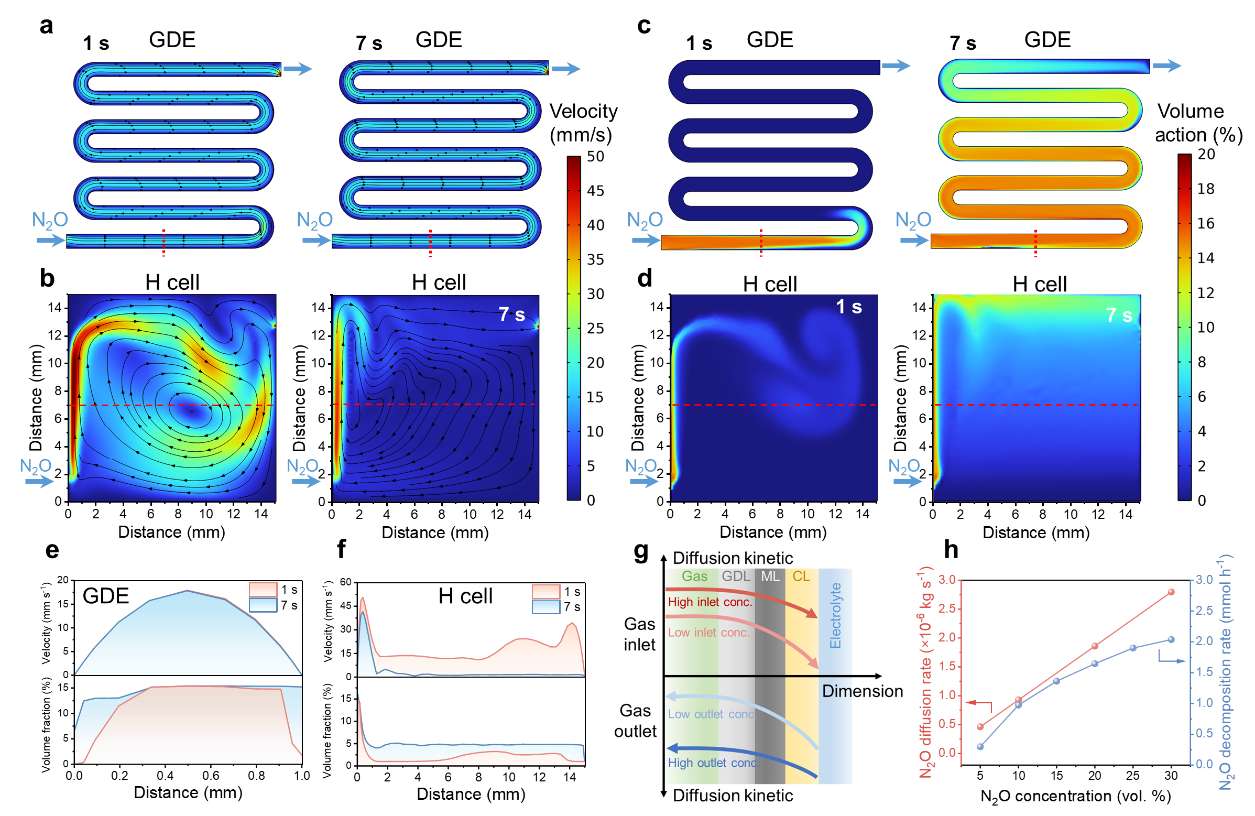
图3 N2O流动状态的CFD模拟。(a)GDE和(b)H型电解池中N2O沿电极表面的流速分布::(c)GDE和(d)H型电解池中N2O沿电极表面的体积分数分布。(e)GDE和(f)H型电解池中N2O流速和体积分数随距离的变化关系。(g)气体从流道到气-液-固三相边界扩散动力的示意图。(h)不同浓度下的N2O理想扩散速率和分解速率。
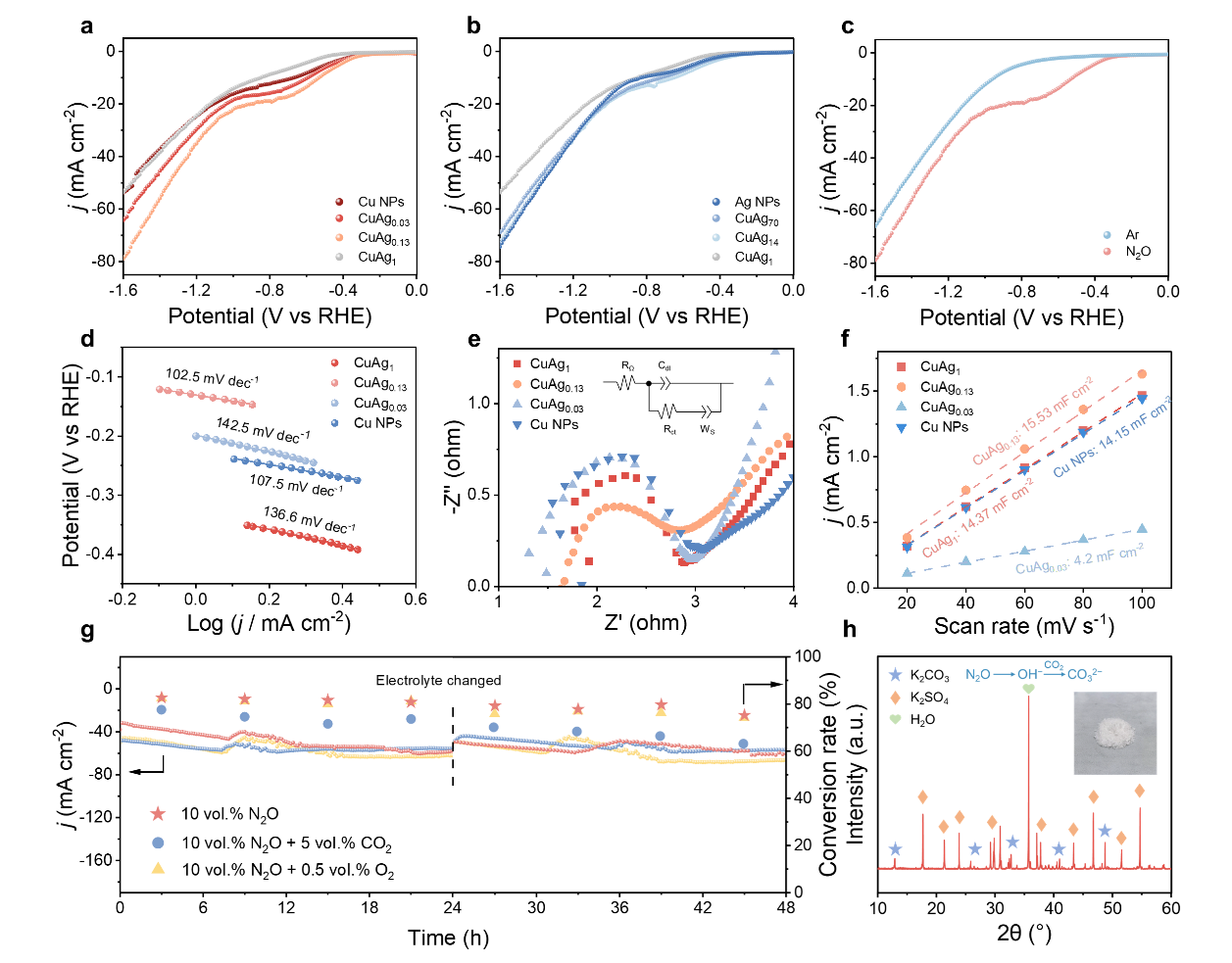
图4 CuAg纳米合金催化剂在N2ORR中的电化学性质。(a-b)不同催化剂在N2O饱和电解质中的LSV曲线。(c)CuAg0.13在Ar和N2O饱和电解质中的LSV曲线。(d)催化剂在N2O饱和条件下的Tafel斜率、(e)Nyquist图和(f)Cdl测量结果。(g)CuAg0.13在不同气体氛围下48小时内的电流密度和N2O转化率。(h)反应后电解质的XRD图谱。
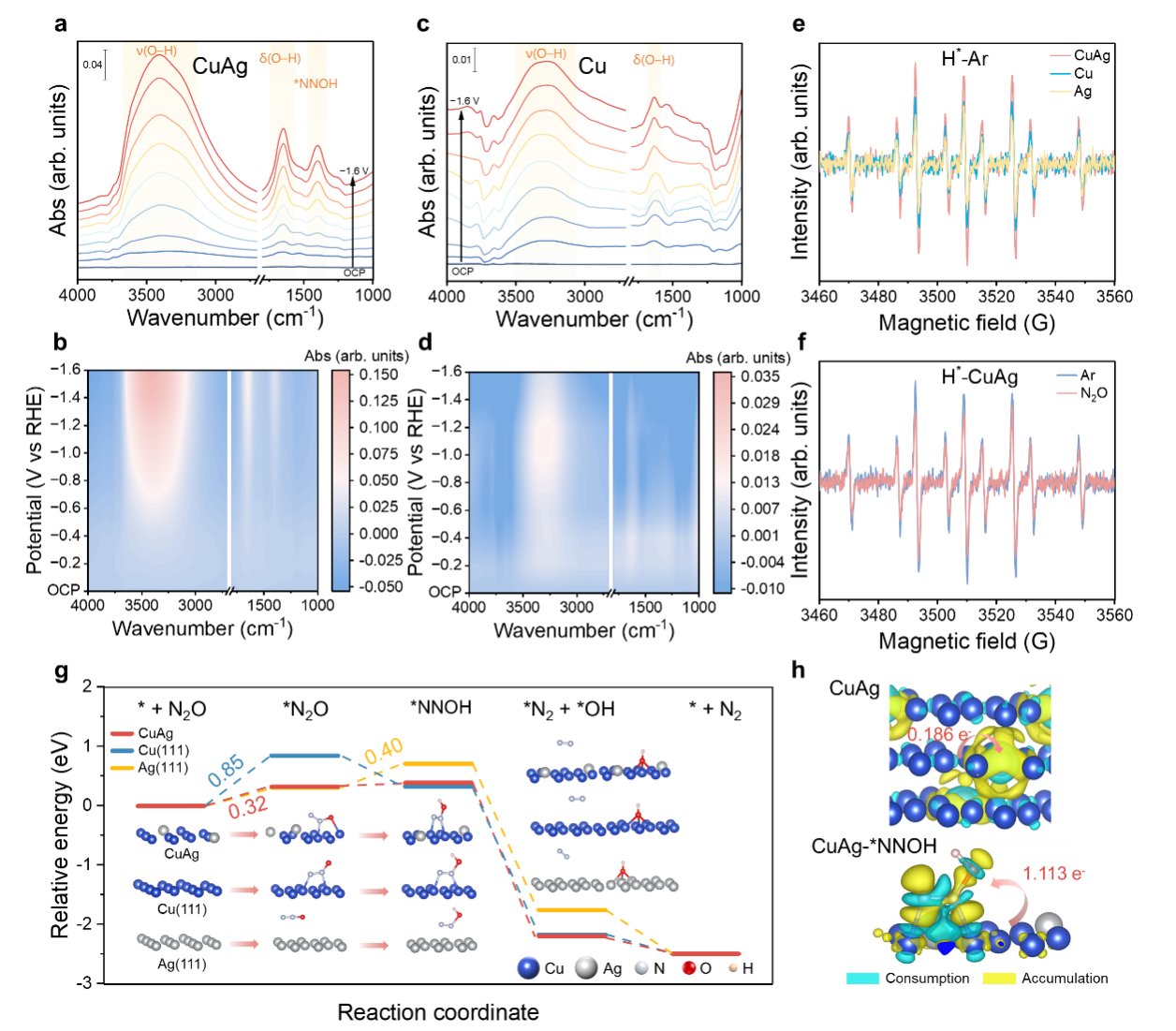
图5 N2ORR的机理分析。(a,b)CuAg和(c,d)Cu上N2ORR的原位DRIFTS光谱。(e)CuAg、Cu和Ag在N2O饱和条件下的活性氢EPR谱。(f)CuAg在Ar和N2O饱和条件下活性氢EPR谱。(g)N2ORR在CuAg、Cu(111)和Ag(111)上的自由能图和中间体构型。(h)CuAg和CuAg-*NNOH的差分电荷密度图。
图6 N2O分解技术的技术经济评估。(a)N2ORR在实验电位范围内的N2O降解平准化成本(LCN2O)。(b)LCN2O的成本分布与(c)敏感性分析。LCN2O依赖于(d)FEN2ORR和电流密度(转化率为80%)以及(e)FEN2ORR和转化率(电流密度为100 mA cm⁻²)的等高线图。(f)多参数优化综合降低LCN2O的路线图。